お知らせ
感染症情報
研究・検査・病原体管理
サーベイランス
刊行・マニュアル・基準
- 詳細
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
- 詳細
 |
国立感染症研究所インフルエンザウイルス研究センター第一室
全国地方衛生研究所 |
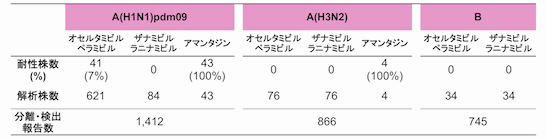
| ・ | ペラミビル治療患者からのH275Y耐性ウイルス検出事例報告 |
| ・ | 新型インフルエンザ(A/H1N1pdm)オセルタミビル耐性株(H275Y)の国内発生状況 [第2報] |
| ・ | 新型インフルエンザ(A/H1N1pdm)オセルタミビル耐性株(H275Y)の国内発生状況 [第1報] |
| ・ | 2008/09インフルエンザシーズンにおけるインフルエンザ(A/H1N1)オセルタミビル耐性株(H275Y)の国内発生状況 [第2報] |
| ・ | 2008/09シーズンにおける季節性インフルエンザ(A/H1N1)オセルタミビル耐性株検出情報 |
| ・ | 2007/08シーズンにおけるインフルエンザ(A/H1N1)オセルタミビル耐性株(H275Y)の国内発生状況 [第2報] |
- 詳細
(掲載日 2014/2/25)
マダニ媒介性の重症熱性血小板減少症候群(SFTS)は、2013年1月に国内の患者が初めて確認された新興ウイルス感染症である。これまでに患者の発生した自治体は、九州・四国・中国・近畿地方の13県(兵庫、島根、岡山、広島、山口、徳島、愛媛、高知、佐賀、長崎、熊本、宮崎及び鹿児島県)である。
SFTSウイルス(SFTSV)が分布する地域では、マダニとマダニに吸血される動物との間でSFTSVが循環・保持される仕組みが成立している。ヒトはSFTSVを保有するマダニに咬まれることで感染する。動物はSFTSVに感染しても発症しないが、感染すると抗体ができる。日本国内には、47種のマダニが生息する。SFTSVの国内分布状況を把握し、その自然界での生活環を明らかにすることは、 SFTS患者発生のリスクを評価し、効果的な感染予防対策を立てる上で非常に重要である。
2013年5月から開始された厚生労働科学研究「SFTSの制圧に向けた総合的研究(研究代表者 倉田 毅)」において、マダニからのSFTSV遺伝子検出法および動物のSFTSV抗体測定法が開発された。これらの検査法により、既に患者が発生している地域だけでなく、患者の発生のない地域も含めて、これまでに入手できたマダニや動物血清の検体を用いて調査を実施したところ、以下のことが明らかになった。
1)マダニについて:九州から北海道の26自治体において、植生マダニ(植物に付着し、動物やヒトを待ち構えているマダニ)とシカに付着しているマダニ(18種4,000匹以上)を調査したところ、複数のマダニ種(タカサゴキララマダニ、フタトゲチマダニ、キチマダニ、オオトゲチマダニ、ヒゲナガチマダニ等)から、SFTSV遺伝子が検出されたが、保有率は5~15%程度とマダニの種類により違いがあった。また、これらのSFTSV保有マダニは、既に患者が確認されている地域(宮崎、鹿児島、徳島、愛媛、高知、岡山、島根、山口、兵庫県)だけではなく、患者が報告されていない地域(三重、滋賀、京都、和歌山、福井、山梨、長野、岐阜、静岡、栃木、群馬、岩手、宮城県、北海道)においても確認された。調査できたマダニ数が数匹と少なかったため、現時点では判断できなかった3自治体(福岡、熊本、福島県)を除くと、調査した全ての自治体でSFTSV遺伝子を持つマダニがみつかったことから、SFTSV保有マダニは調査していない自治体を含めて国内に広く分布していると考えられる。
2)動物のSFTSV抗体保有状況について:保存血清等を用いて調査した前回の調査[SFTSウイルスの国内分布調査結果(第一報)http://www.niid.go.jp/niid/ja/sfts/sfts-iasrs/3864-pr4043.html]に加えて、平成25年度にシカ(16自治体)、イヌ(2自治体)のSFTSV抗体調査を行った。その結果、シカでは、前回の調査と併せて検体が得られた地域(27自治体)のうち、17自治体(福岡、熊本、宮崎、鹿児島、島根、広島、山口、徳島、愛媛、三重、滋賀、京都、兵庫、和歌山、長野、静岡、宮城県)でSFTSV抗体陽性のシカが確認されたが、その他の10自治体(大分、高知、岐阜、山梨、栃木、群馬、千葉、岩手、福島県、北海道;ただし大分、高知、千葉、福島県は、それぞれ3、1、5、4頭しか調査されていない)では陽性のシカは今回の調査ではみつからなかった。また、シカにおける抗体陽性率は、0%(抗体陽性動物みつからず)から最大で90%と地域差が大きく(陽性シカがみつかった地域での平均は31%)、特にSFTS患者発生地域およびその近隣地域で抗体陽性率が高い傾向がみられた。イヌでは、検体が得られた地域(19自治体)のうち、九州(熊本、宮崎、鹿児島県)、四国(徳島、香川、愛媛、高知県)以外に、患者が報告されていない自治体(三重、富山、岐阜県)でも抗体保有動物が存在した。一方、9自治体(沖縄、長崎、広島、滋賀、愛知、静岡、長野、新潟県、北海道)では陽性のイヌはみつからなかった。
本病の発生が先に報告された中国では、SFTSVの主な媒介マダニはフタトゲチマダニとされ、また、ヤギ、ヒツジ、ウシ、イヌ等の動物がSFTSVの抗体を高率に保有していることから、フタトゲチマダニとこれらの動物との間でSFTSVの生活環ができていると考えられている。一方、日本では、少なくともフタトゲチマダニとタカサゴキララマダニがSFTSVを媒介すると考えられている。今回の調査結果から、これら2種のマダニ以外にもSFTSVを保有するマダニ(特にチマダニ属)が複数種存在することが分かった。今回の調査は、前回の調査[SFTSウイルスの国内分布調査結果(第一報)http://www.niid.go.jp/niid/ja/sfts/sfts-iasrs/3864-pr4043.html]をさらに拡大して実施されたものであり、より多くの地域を対象とした。未だ、マダニ、動物とも全国を網羅的に調査されてはいないが、SFTSV保有マダニは調査していない自治体を含めて国内に広く分布していると考えられる。
今後、研究班としては、各自治体や関係者の協力を得ながら、対象地域や検体採取地点、動物の種類・頭数を広げて調査を実施することにより、マダニと動物におけるSFTSVの生活環をより詳細に解明したい。
なお、今回の調査にあたって御協力をいただいた、大日本猟友会ならびに徳島県他多くの自治体関係者の皆様に深謝申し上げます。
国立感染症研究所 獣医科学部
森川 茂 宇田晶彦 木村昌伸 藤田 修 加来義浩 今岡浩一
同 昆虫医科学部 澤辺京子
同 細菌第一部 川端寛樹
同 ウイルス第一部 安藤秀二 西條政幸
山口大学共同獣医学部 前田 健 高野 愛
岐阜大学応用生物科学部 柳井徳磨
馬原アカリ医学研究所 藤田博己
福井大学医学部 高田伸弘
厚生労働省結核感染症課 中嶋建介 福島和子
- 詳細
| 国立感染症研究所・感染症情報センターには地方衛生研究所(地研)から「病原体個票」が報告されている。これには感染症発生動向調査の定点およびその他の医療機関、保健所等で採取された検体から検出された病原体の情報が含まれる(参考図)。 |
|
|||||
|
*2013/14シーズンは2013年第36週/9月~2014年第35週/8月(検体採取週)。 図の元データは、以下の速報グラフ(病原体個票による報告)。 データは、土日祝日を除く2日前に地研から報告された情報。過去の週に遡っての追加報告もある。現在報告数は、地研より報告された日を表す。
|
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
- 詳細
(IASR Vol. 35 p. 48-49: 2014年2月号)
東京都健康安全研究センターでは、感染症発生動向調査事業の一つとして、都内の内科病原体定点医療機関(15定点)から提供されるインフルエンザ様症状を示す患者検体の検査を行っている。2013年第35~36週(8月26日~9月8日)に採取された2検体から、国内では非常に検出の稀なコクサッキーウイルスA群21型(以下CA21と略)が検出されたので報告する。
検体は、第35週および第36週に23区内の異なる区から咽頭ぬぐい液が各1検体ずつ搬入された。患者(39歳、17歳)は、いずれも発熱(38.3℃、39℃)、筋関節痛、上気道炎等の風邪様症状を呈していた。患者の発症前行動は、約2週間前にフィリピンへの渡航歴がある例と国内に滞在していた例で、両者に共通性は無かった。また、患者の発症時期から推定すると、両例とも国内における感染が強く疑われた。
病原体検索は、エンテロウイルスの遺伝子検査として、ノンコード領域に設計されたスクリーニング検査用プライマーを用いてPCRを行い、増幅産物の配列をNCBIのBlastで相同性検索した結果、CA21の配列に最も近いことが明らかとなった。このためエンテロウイルスの遺伝子型別として有用なVP1領域に設定されたCODEHOP PCR法1)プライマーを用いてVP1領域を増幅し、得られた315bpの塩基配列について相同性検索を行ったところ、CA21ウイルス(JN169053.1)と98%の相同性で一致した。また、エンテロウイルスC種を中心としたVP1遺伝子を用いた遺伝子系統樹解析の結果では、検出された2例ともCA21のクラスターに入ることが確認された (図1)。
一方、A549細胞を用いたウイルス分離試験においても、本事例株はエンテロウイルスに特徴的なCPE(細胞変性効果)を示したが、既存のエンテロウイルスプール血清を用いた中和試験では該当する型が認められなかった。国立感染症研究所ウイルス第二部第二室(エンテロウイルス室)より分与されたエンテロウイルスC種に分類された単味抗血清数種を用いて中和反応を試みたところ、抗CA21血清(20単位で使用)で観察2日までに中和された株と、観察2日目までは抗CA21および抗CA24血清(20単位で使用)で発育阻止を起こしたものの観察4日目に抗CA21のみの中和を確認した株が認められたことから、これらをCA21株と同定した。
CA21ウイルスの国内の検出報告は少なく、特に臨床材料からの報告は1986年に埼玉県の刑務所施設での発生例以来27年ぶりとなる。海外では2006~2010年に中国で行われた調査で患者の26.2%からCA21が検出されており2)、フィリピン等でもウイルスの検出報告がある3)。また、環境材料(下水検体)からは2010年、2011年に福岡で検出が報告されていることから、今後、国内での発生が危惧されるウイルスの一つといえる。都内では、本例以降、病原体定点検体からCA21は検出されていないため、ウイルスの伝播および拡散は発生しなかったことが推察される。しかし、都内の異なった地域での複数例の感染は、今後のエンテロウイルス発生動向を調査する上で留意する点となった。
参考文献
1) J Clin Microbiol 44: 2698-2704, 2006
2) Emerg Infect Dis 18: 821-824, 2012
3) Virus Genes 45: 207-217, 2012
東京都健康安全研究センター微生物部
新開敬行 原田幸子 吉田 勲 長島真美 林 志直 甲斐明美
- 詳細
2013年に手足口病患者から検出されたコクサッキーウイルスA6について―仙台市
(IASR Vol. 35 p. 49-50: 2014年2月号)
2013年、仙台市における手足口病の定点当たりの患者報告数は第25週から増加し始め、第34週でピークに達した後減少した。ピーク時の報告数は定点当たり6.46人で、2012年(6.12人)とほぼ同じ小規模の流行となった。
ウイルス分離・同定は、病原体定点で採取された咽頭ぬぐい液をRD-A細胞に接種後37℃1週間培養し3代目まで継代した。細胞培養にてCPEが認められた検体については、培養上清を精製後、国立感染症研究所から分与された抗血清で中和試験を試みた。中和試験により血清型を決定できなかった分離株については、塩基配列の解析(VP1およびVP4領域)により決定した。また、検体(咽頭ぬぐい液)から市販のキットを用いてRNAを抽出し、CODEHOP PCR法1)によりVP1領域の遺伝子を増幅した。増幅産物を精製後、ダイレクトシークエンス法により塩基配列を決定し、血清型の同定を行った。
手足口病患者の検体(咽頭ぬぐい液)は、非流行期の2012年12月~2013年1月にかけて3検体が搬入され、細胞でのCPEは観察されなかったが、遺伝子検査によりコクサッキーウイルスA6(CVA6)遺伝子が検出された(表1)。その後、流行開始とともに6月中旬から検体が搬入され始め、10月までに16検体が搬入された。このうち11検体で細胞培養にてCPEが認められ、4検体からの分離株は中和試験によりCVA6と同定された。残り7検体からの分離株も遺伝子解析によりCVA6が6株、CVA2が1株と同定された。一方、遺伝子検査では16検体すべてにおいてCODEHOP PCR法による増幅産物が確認され、遺伝子解析の結果、CVA6遺伝子が14検体から、ライノウイルスが3検体から、CVA2が1検体から検出された。このうち2検体からはCVA6遺伝子とライノウイルス遺伝子が同時に検出された(CODEHOP PCR法による増幅産物はエンテロウイルスが376bpであるのに対し、ライノウイルスは330bpで、混合感染の場合、2本のバンドが検出された)。
検出されたCVA6のVP1領域の系統樹解析の結果、増本らが報告2)した2011-Japan-B のクラスターに属する遺伝子が4検体から検出されたが、残り10検体から検出されたCVA6遺伝子は、清田ら3)が報告した2013-Kumamotoと同一クラスターに分類された。また、2名のヘルパンギーナ患者検体から検出されたCVA6の遺伝子もこのクラスターに分類された(図)。
2011年に国内でCVA6による手足口病が流行した際、仙台市内で検出されたCVA6は、遺伝子解析の結果、5検体すべて2011-Japan-A のクラスターに属していた。新しいクラスターに属するCVA6は、2012年8月にヘルパンギーナと診断された検体から検出されたのが最初で、2012年12月~2013年1月の非流行期の手足口病の検体から検出された遺伝子もこのクラスターに属していた。また、清田ら3)が報告した2013-Kumamotoと同一クラスターに分類されたことから、今シーズンのCVA6は新しいタイプが流行したものと思われる。さらに、2013年7月以降に搬入された多くの検体でRD-A細胞においてCPEが認められ、ウイルス分離が可能であったことから、2011年に流行したCVA6と大きな違いがみられた。今後は、非流行期も含め、手足口病から検出される病原体の動向に注意する必要があると考える。
参考文献
1) Allan W, et al., J Clin Microbiol 44: 2698-2704, 2006
2) IASR 33: 60-61, 2012
3) IASR 34: 233, 2013
仙台市衛生研究所
千田恭子 菅原瑶子 関根雅夫 中田 歩 勝見正道 小林正裕
長谷川小児科医院 長谷川純男
かやば小児科医院 萱場 潤