(IDWR 2003年第24号)
人や物資の世界的規模の交流により、今まで我々に無縁と思われていた病原性の強い微生物による「輸入感染症」の危険性が高まっている。微生物感染 の中で皮膚糸状菌症以外の真菌症はヒトからヒト、動物からヒトへの直接感染は否定されており、この「輸入感染症」の対象から外されていた。しかし、真菌症 でもコクシジオイデス症(coccidioidomycosis )の病原性はペストに相当し、極めて強い。本症は4 類感染症全数把握疾患に指定された唯一の真菌症である。
疫 学
コクシジオイデス症は米国西南部(カリフォルニア、アリゾナ、テキサス、ネバダ、ユタの諸州)、メキシコ西部、アルゼンチンのパンパ地域、ベネズエラのファルコン州の半乾燥地域の風土病で、渓谷熱(valley fever)、砂漠リューマチ(desert rheumatism)あるいは砂漠熱(desert fever)とも呼ばれている。これら半乾燥地帯の限られた地域の土壌中に原因真菌であるCoccidioides immitis Rixford et Glichrist 1896(コクシジオイデス・イミチス)が生息し、その分節型分生子は強風や土木工事などで空中に舞い上がり、これら分生子を吸入することにより肺に感染 を起こす。毎年多数発生する患者の約0.5%は全身感染に波及し、その半数が致死的となる。C. immitis の病原性はペスト菌に相当する。本症が日本で発症した場合、菌の同定には特別な注意が必要である。本菌は菌糸状発育しているシャーレの蓋を不用意に開けた だけで、分生子が空中に舞い上がり室内を汚染する。患者と直接接触する医師や看護師より、患者の検体から培養された真菌を取り扱う検査技師や研究者に二次 感染の危険がある。米国では過去に200名近い研究者および臨床検査技師が感染を経験しており、死亡例も少なくない。
本邦では2002年9月までに31例が報告されており、カリフォルニア州やアリゾナ州への海外渡航歴を有するものが大部分ではあるが、2例は渡航歴のな い綿花を扱う工場の従業員で、輸入された綿花に付着した原因菌を吸入したことにより感染したと考えられる。
病原体
1. 原因菌
C. immitis は、取り扱い上最も危険な真菌である。本菌の有性世代は不明である。普通の培地上では菌糸形を、生体内及び特殊な培養法で培養すると内生胞子(endospore )で満たされた球状体(spherule)を形成する。集落の形態は初め無毛で灰白色、次第に白色綿毛状となる。しかしながら淡褐色を呈する菌株もかなり多く、粉状になるものもある。発育は速く、27 ℃より37 ℃の方がよい。顕微鏡的には、菌糸は培養するにつれ菌糸内に多数の隔壁ができ、細胞質が消失した解離細胞(disjunctor cell)と分節型分生子が交互に連なる状態になる。分節型分生子は矩形から樽型(2.5 〜3×4 〜6 μm)である。自然界では条件が違うと分節型分生子が発芽し、菌糸となる。
2. 病態生理
吸入により生体内に入ったC. immitis の分節型分生子は球状に腫大し、球状体となる。初期の球状体は内外の2層に分かれる。外層は細胞質より成り、内層は多糖体様物質で満たされているが、発育 するにつれ消失する。球状体の腫大とともに細胞質膜、次いで細胞壁が中心に向かって折れ込むように発達し、以後球状体の発達とともに連続的に分葉し、細胞 質を無数の小室に分けていく。
|
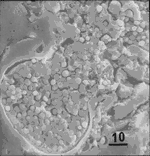
続いて個々の小室内にいくつかの内生胞子が現れ、内生胞子の成熟とともに周囲の組織は融解し、最後には無数の内生胞子(2 〜5 μm)が充満した球状体(40〜2,000 μm )が形成される。やがて球体内の壁の一部が破れ、内生胞子は組織中に放出される(写真1)。これら内生胞子は腫大して球状体となり、同じサイクルを繰り返す。なお、感染した分節型分生子が成熟した球状体となり、内生胞子が組織中に放出されるまでの期間は約5日である。 |
|
|
写真1. マウス肝臓における C.immitis :球状体から放出された内生胞子 |
臨床症状
1. 原発性肺コクシジオイデス症 primary pulmonary coccidioidomycosis
ほとんど無症状であるが、約40%において、軽いカゼに似た症状を示す。汚染地域の住民のほとんどは短期間に自然治癒する。特徴的なこととして、約10%の患者(女性に多い)の下腿に紅斑を伴う結節(結節性紅斑 erythema nodosum )が見られる。
2. 原発性皮膚コクシジオイデス症 primary cutaneous coccidioidomysosis
極く稀に皮膚に初発病巣が生じる。刺傷あるいは外傷により感染し、発症する。潰瘍を形成し、花キャベツ状の腫瘤となる。
3. 良性残留性コクシジオイデス症 benign residual coccidioidomycosis
症状がみられた原発性コクシジオイデス症の2〜8%の患者の肺に、結核に似た空洞が形成される。空洞壁は薄く嚢腫状を呈し、液を貯留していることもある。炎症反応はほとんどない。病巣はそれ以上進行せず、感染の恐れもない。自覚症状はほとんどなく、X 線撮影によってのみ見いだされる。別名コクシジオイドーマ(コクシジオイデス腫coccidioidoma )と呼ばれることもある。
4. 播種性コクシジオイデス症 disseminated coccidioidomycosis
別名コクシジオイデス肉芽腫coccidioidal granuloma 。進行性あるいは2次性コクシジオイデス症progressive or secondary coccidioidomycosis ともいわれている。肺の初感染病巣が進行し、血行性に全身に散布する。原発性肺コクシジオイデス症の患者の約0.5%に発生し、そのうち約半数が死の転帰 をとる。免疫不全の患者に起こることが多い。皮膚、皮下組織、骨、関節、肝、腎、およびリンパ組織が侵される。なお、急性の場合、髄膜炎 (coccidioidal meningitis)を併発することが多い。
病原診断
1. C.immitis の分離同定
当然のことながら、本菌の分離同定作業は隔離された安全キャビネット内で行われなければならない。本菌の同定の決め手は(1)37 ℃における旺盛な発育、(2 )培地上での分節型分生子の形成、(3)特殊培養あるいは動物実験による球状体の確認である。
C. immitis の旺盛な発育を観察するには、通常使用されている真菌および細菌用培地が用いられる。汚染菌を防ぐ目的で添加されるクロラムフェニコールやシクロヘキシミ ド(cycloheximid)によって発育は阻害されない。通常サブロー・ブドウ糖寒天培地が使用されている。慎重に菌を培地中央部に接種し、シャーレ の蓋と本体をビニールテープで密封し、さらに透明プラスチック容器に入れて孵卵器に入れて観察する。37 ℃で7 日後に直径40mm 以上の集落となる。
分節型分生子は、1%の割合でブドウ糖を添加したブレインハートインフュージョン斜面寒天培地に菌を接種し、37 ℃で培養すると10 日前後で形成される。観察法は試験管を顕微鏡の鏡台に横たえ、管壁越しに行う。分節型分生子は僅かな空気の動きでも飛散するので、斜面培地の蓋をとっては ならない。通常の真菌で用いられている乗せガラス培養法(slide culture)は大変危険なので、行ってはならない。DNA 抽出も斜面培地の栓より70%エタノールや10%ホルマリンなどの固定液を注射筒で注入し、完全に固定されるまで(1 週間以上)注射筒はそのままにし、その後実験に用いる。
球状体の観察は、培地の調整および培養法(炭酸ガス培養、振盪培養装置)が煩雑であること、一般の施設での動物実験は許可されていないことなどから、特定の研究機関に依頼されることを推奨したい。なお、女性ホルモンはC. immitis の成長を促進するため、妊婦は本菌を扱ってはならない。
2. 病理組織学的診断
組織内でC. immitis は、内生胞子を内蔵した球状体、および球状体から放出された内生胞子、各種発達段階にある球状体として観察される。染色はPAS およびGMS を推奨する。病理学的特徴は肉芽腫性炎症と化膿性炎症の混じり合った像であるが、どちらが主になるかは病型および菌の寄生形態に左右される。肺の初感染巣 は主に肉芽腫炎症像を示すが、急性全身感染の場合は化膿性炎症像が強くなる。また、球状体の発育段階によっても組織反応は異なってくる。
激しい限局した化膿性炎症像は、球状体から内生胞子が組織内に放出された時に起こり、これら内生胞子が成熟した球状体に変わっていくにつれ、病巣は肉芽腫性へと変わっていく。
3. 免疫学的診断
免疫反応用抗原としてコクシジオイジン(coccidioidin)およびスフェルリン(Spherulin)が開発されている。これらの抗原は遅延型皮膚反応の検出に用いられる。また、ベータ‐1,3 ‐グルカン(β‐1,3‐glucan)を検出するキットもコクシジオイデス症に反応するといわれている。
一方、コクシジオイデス症における血清抗体も種々の方法で検出されている。沈降抗体は通常感染1週間から3週間の間に出現する。これは試験管内沈降試 験、二重拡散法、あるいは免疫電気泳動法で検出可能である。補体結合反応も感染7日以降より陽性となり、病状の悪化とともにその抗体価は上昇し、病状の好 転とともに低下していく。また、ラテックス凝集反応も行われ、この価は試験管内沈降反応の結果と良く一致する。
本症の血清学的診断法としては、補体結合反応と二重拡散法の併用が優れている。二重拡散法の代わりに免疫電気泳動法を用いても良い。なお、中枢神経系のコクシジオイデス症の場合、血清の代わりに脳脊髄液中の抗体価が測定されている。
4. PCR によるC. immitis 遺伝子の検出
2002年9月現在、2,716個のC. immitis の遺伝子がGenBank に登録されている。また、本菌を特異的に検出するプライマーも、28S リボゾームRNA遺伝子や19kDa 抗原遺伝子を使って報告されている。近年中には、血液、髄液、組織標本を用いたC. immitis の遺伝子検出が日常検査で行われるようになる。また、培養菌体を固定してDNA を検出し、遺伝子シーケンスにより同定することはすでに可能である。
治療・予防
播種性コクシジオイデス症の治療は困難である。現在イミダゾール系の抗真菌剤(ケトコナゾール、ミコナゾール、イトラコナゾールなど)、およびフロル化 ピリミジン化合物の一種である5‐フルオロシトシン(5‐FC)が実用に供されているが、古くから使用されているアムフォテリシンB が依然として唯一の確実な治療薬である。アムフォテリシンBの抗真菌作用は優れているが、副作用(肝、腎障害)が強く、使用に当たっては十分な注意が必要 とされている。
感染症法における取り扱い(2012年7月更新)
全数報告対象(4類感染症)であり、診断した医師は直ちに最寄りの保健所に届け出なければならない。
届出基準はこちら
【参考文献】
1. 宮治 誠,西村和子,佐野文子:コクシジオイデス症とその起炎菌.新・土の微生物(8):土のヒト病原菌類.pp25‐32, 博友社(東京)2002.
2. Fujio J, Nishimura K, Miyaji M: Epidemiological survey of the imported mycoses in Japan. Jpn J Med Mycol 40:103‐109,1999.
3. Miyaji M: The imported mycoses. Pathology and Clinical Medicine 9:1301‐1307,1998.
4. Miyaji M: Biohazards caused by imported fungi. Jpn J Med Mycol 34:113‐ 120,1993.
(千葉大学真菌医学研究センター病原真菌研究部門 宮治 誠)