(2013年03月07日改訂)
マラリア(Malaria)は、亜熱帯・熱帯地域を中心に感染者数が多く、世界的に重要な感染症である。また、非流行地から流行地を訪れる旅行者でも問題となるが、その場合、流行地とは異なった視点での対応も必要となる。感染したマラリア原虫の種によって、病型や治療法も異なるが、熱帯熱マラリアでは、早期に適切な対応をしないと、短期間で重症化し死に至ることがある。
疫学
マラリアは100カ国余りで流行しており、世界保健機構(WHO)の推計によると、年間2億 人以上の罹患者と200万人の死亡者がある1)。死亡例の大部分はサハラ以南アフリカにおける5歳未満の小児だが、アフリカ以外に、アジアや南太平洋諸国、中南米でも多くの発生がみられる。重症化しやすく死亡率も高い熱帯熱マラリアは、アフリカやアジア・太平洋の熱帯地域が流行の中心だが、三日熱マラリアは、韓国や中国といった温帯地域でも問題になっている。黒人は遺伝的に三日熱マラリア原虫に感染しにくく、従来、三日熱マラリアの流行は、アフリカではないとされたが、アジア系住民の流入増加もあり、東アフリカを中心に報告されるようになった。熱帯熱マラリアと三日熱マラリアの両方がみられる地域では、マラリア対策の進捗により、流行の中心が熱帯熱マラリアから三日熱マラリアに移る現象がみられ、現在、東南アジアや中南米ではマラリア患者数が減少するとともに、相対的に三日熱マラリアの比率が増している。卵形マラリアや四日熱マラリアは、熱帯熱マラリアや三日熱マラリアに比して感染者は少ない。
旅行医学の領域でもマラリアは重要な疾患で、全世界では、旅行者が帰国してから発症する例が年間3万人程度あるとされる。マラリアに対して免疫がない旅行者では、診断・治療の遅れで致死的となるので、的確な早期対応が求められる。日本国内での報告数は、1990年代は増加傾向を示し、2000年には年間154例に達したが、最近は年間50~70例で推移している。国内での報告例は輸入例に限られるが、推定感染地域の流行事情を反映し、アジア地域での感染例では三日熱マラリア、アフリカ地域での感染例では熱帯熱マラリアが多い2)。輸血(保存血、血小板、交換輸血)、針刺し事故などによる感染も起こり得るので、検査検体を取り扱う際も注意を要するが、日本国内では、1991年の輸血マラリアを最後に、輸入例以外の報告はない。また、マラリア原虫を媒介するハマダラカ(Anopheles属の蚊)は、日本国内にも生息しており、同じように国内に媒介蚊が生息するデング熱やチクングニア熱と同様、マラリアも検疫感染症に指定されている。もっとも、最近の日本国内での温暖化傾向にあっても、媒介蚊の生息地拡大や生息数増加を示唆する報告は少なく、国内でのマラリア再興のリスクは小さい3)。
病原体
マラリアの病原体はPlasmodium 属の原虫で、ヒトに感染して臨床的に問題となるのは、熱帯熱マラリア原虫(P. falciparum)、三日熱マラリア原虫(P. vivax)、卵形マラリア原虫(P. ovale)、四日熱マラリア原虫(P. malariae)の4種とされてきたが、2004年以降、マカク属のサルで感染が問題となっていたP. knowlesiのヒトでの集団感染例が、マレーシア、ボルネオ島で明らかになった。以後、媒介蚊であるAnopheles leucosphyrus が生息するインドシナ諸国、フィリピンなどから感染例の報告が続き、2012年には、マレーシアから帰国した日本人での発症例も報告された4) 5)。
メスのハマダラカが産卵のため吸血する際、唾液腺に集積していたマラリア原虫のスポロゾイトは、唾液注入に伴い体内に侵入する。血中に入ったスポロゾイトは45分程度で肝細胞に取り込まれるが、肝細胞内で分裂を開始し、数千個のメロゾイトになった段階で肝細胞を破壊して血中に放出される。メロゾイトは赤血球に侵入し、輪状体(早期栄養体)、栄養体(後期栄養体、あるいはアメーバ体)、分裂体の経過をたどり、8~32個に分裂した段階で赤血球膜を破壊して放出され、メロゾイトは新たな赤血球に侵入して上記のサイクルを繰り返す。三日熱マラリア原虫と卵形マラリア原虫の場合には、肝細胞内で休眠体(ヒプノゾイト)が形成された後、長期間経過してから分裂を開始して血中に放出され、症状が再発することがある。
無性生殖を繰り返すうちに、一部の原虫は雌雄の区別がある生殖母体ヘと分化する。これはヒト体内では有性生殖をしないが、ハマダラカに吸われるとその中腸内で合体受精して最終的にオーシストとなり、その中に多数のスポロゾイトが形成される。このマラリア原虫感染蚊の吸血で、ヒト-蚊-ヒトのマラリア原虫感染サイクルが完結するが、従来から知られた4種の原虫と異なり、P. knowlesiについては、サル-蚊-ヒトでの感染サイクルは確認されているものの、ヒト-蚊-ヒトでの自然感染はまだ確認されていない4)。
病態・臨床症状
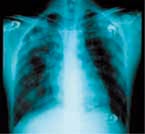
マラリア流行地で育ったわけではなく、マラリアに免疫のないヒト(non-immune)が初感染した場合、発熱はほぼ必発といってよく、原虫侵入後の潜伏期は熱帯熱マラリアで12日前後、四日熱マラリアは30日前後、三日熱マラリアと卵形マラリアでは14日前後である。ただし、流行地で生まれ育ち、何度もマラリアに罹患して免疫を得ているヒト(semi-immune)では、発熱などの症状が軽度しかみられないこともある。また、三日熱マラリアでは、non-immuneでも1年以上、はっきりした症状もなく過ごすことがある。 典型例では、潜伏期間の後、悪寒、震えと共に熱発作で発症する。この熱発作の間隔は、四日熱マラリアで72時間ごと、三日熱・卵形マラリアで48時間ごと、熱帯マラリアでは不定期で短い。P. konowlesi感染では24時間程度と言われている。発熱に伴い、倦怠感、頭痛、筋肉痛、関節痛などがみられるが、腹部症状(悪心・嘔吐、下痢、腹痛)や、呼吸器症状がめだつこともあり、マラリアを疑わないと、風邪やインフルエンザと誤診されることになる。一般検査所見では血小板減少、LDH上昇などが高頻度にみられる。貧血は、病初期にはみられないことも多い。熱帯熱マラリア原虫が感染した赤血球は、表面に種々の原虫由来物質を表出するので、細血管に富む臓器を中心に、血管内皮への血球の固着が多臓器不全を起こす。重症化すると脳症、腎症、肺水腫/ARDS(図1)、DIC様出血傾向(図2)、重症貧血、代謝性アシドーシス、低血糖、黒水熱(高度の血色素尿症)など種々の合併症を生じ、致死的となる6)。熱帯熱マラリア以外でも、最近、三日熱マラリアでも呼吸器症状などの臓器障害を合併する例が報告されており、注意が必要である。
 |
 |
|
図1. 重症マラリア症例における肺水腫/ARDSの胸部レ線像。両肺野全体に異常陰影があるが、特に右肺に顕著である。 |
図2. 重症マラリア症例における出血傾向。左上肢に広範な出血斑がみられる。 |
診断
 |
|
表 各種マラリア迅速診断キットと使用抗原 |
血液塗抹標本を染色し、光学顕微鏡で検査する形態学的診断法がgold standardである。塗抹標本には厚層塗抹と薄層塗抹があり、理論上は厚層塗抹の方が多くの血液量を検査できるので診断感度が高く、途上国のマラリア流行地ではよく行われる。日本国内では、一般的な血球の形態検査と同様、複数の血液薄層標本を作製し、ギムザ染色して鏡検するのが実際的である。血液塗抹標本で見られる熱帯熱マラリア原虫は通常、輪状体のみであり、数が少ないときなど見逃しやすい。形態診断では、アクリジン・オレンジ染色の併用も有用だが、顕微鏡検査での診断精度は、検査者の経験と技量によるところが大きいので、マラリアが強く疑われる場合、他の検査法も併用することが望ましい。
マラリアの迅速診断キットは、顕微鏡による診断が困難な流行地のヘルス・ポストのみならず、非流行国でのトラベル・クリニックなどでも広く利用され、現在100種類以上のキットが販売されている。ただし、その品質はまちまちで、WHOは、原虫密度100/μl以上での検出を基準としている7)。イムノクロマト法によってマラリア原虫特異抗原を検出するという原理は共通だが、histidine-rich protein 2 (HRP-2)を検出するキットおよび,マラリア原虫の細胞内代謝酵素plasmodium lactate dehydrogenase (pLDH)を検出するキットに大別される(表)。どのキットも、致死的となり得る熱帯熱マラリアと他のマラリアをマラリア原虫とを、15分程度で区別して検出できることを一義的に考えている。一般的に、熱帯熱マラリア原虫の検出には、HRP2検出系がすぐれ、三日熱マラリア原虫の検出にはpLDH検出系がすぐれているので、最近、複数の抗原を使用するキットも臨床応用されている。ただし、原虫密度50/μl以下程度となると、検出率は極端に低下する傾向は同じである 8)。また、日本国内で臨床試験薬として認可されている製品はなく、国内での使用については、顕微鏡的形態検査などによる確定診断の補助として用いるのが原則である。
PCR法としてはrRNA遺伝子を標的にした鑑別法が木村やSnounouらによって開発されている9) 10)。木村らの方法は4種のマラリア原虫の特異的なrRNA遺伝子配列のうち、それぞれ約100bpを増幅する。Snounouらの方法は、異なる長さのPCR産物が増幅できるので種の鑑別には便利だが、卵形マラリアの亜種が検出できないことに注意すべきである11)。 P. knowlesiの検出には、三日熱マラリアとの交差反応を避けるために、rRNA 遺伝子とCSP遺伝子を組み合わせた2種類のPCRで判別をすることが必要である12)13)。PCR法には、ある程度の設備と技術が必要ではあるが、5種類のマラリア原虫を区別して感度良く検出でき、顕微鏡法を補うものとして、あるいは顕微鏡法の技術を高めるものとして有用である。
さらに、実際の診断にあたっては、患者の行動歴や臨床情報とならんで世界的なマラリアの疫学的状況の把握も重要となる。熱帯地域から帰国後の熱性疾患では、デング熱などのアルボウイルス感染との鑑別が重要だが、マラリア原虫を媒介するAnopheles属の蚊は、アルボウイルスを媒介するAedes属の蚊と異なり、都市環境では生息できない。アフリカやインド等の一部の国を除き、日本人が、熱帯の都市に滞在しマラリアに罹患する可能性はかなり低い。また、発熱以外に消化器症状が前面に出た場合は、腸チフスとの鑑別が問題となる。
治療(予防投薬を含む)
マラリアの治療は、急性期治療と根治的治療に分けて考えることができる。世界的にみると、従来からクロロキン耐性が問題となっていた熱帯熱マラリア以外のマラリアでも、急性期の治療薬として、短期作用型のアルテスネートと長期作用型の他剤を組み合わせた合剤が利用されることが多くなった。熱帯熱マラリアの合併症に対し、病態に合わせた補助的治療が必要なのは、他の重症疾患と同じである。また、三日熱マラリアと卵形マラリアの場合は、急性期治療の後に、肝細胞内に潜む休眠体原虫を殺滅する根治療法として、プリマキンの投与が必要となる。
日本国内での治療を考えた場合、三日熱マラリア、卵形マラリア、四日熱マラリア、P. knowlesiでの急性期治療としてクロロキンを用いてもよいが、三日熱マラリアではパプアニューギニア、インドネシアなどでクロロキン耐性が出現していることも念頭におく14)。クロロキンが入手不可能な場合は、国内市販薬であるスルファドキシン/ピリメタミン、メフロキンなどを用いることになる。熱帯熱マラリアではクロロキン耐性が進行しているので、クロロキン以外の薬剤を用いるべきだが、スルファドキシン/ピリメタミン合剤も耐性が進行しつつある。メフロキンは、タイ・カンボジアあるいはタイ・ミャンマーなどの国境地帯の感染を除けば、有効なことが多い。インドシナ半島の流行地では、熱帯熱マラリアで多剤耐性が進行しているので、クロロキンやスルファドキシン/ピリメタミン合剤以外の薬剤を用いた方がよい。マラリア流行地では、最近、アーテメター/ルメファントリン合剤の使用機会が増えており、欧米でも使われ始めたが、日本ではまだ認可されていない。欧米ではキニーネ経口薬とドキシサイクリン、あるいはクリンダマイシンとの併用も行われる。薬剤耐性熱帯熱マラリアに有効な薬剤としては、最近、国内ではアトバコン/プログアニル塩酸塩が、新たに治療薬として認可された。
重症マラリアでは非経口的な投与が必要であり、キニーネ注射薬が標準的だが、最近ではアーテミシニンおよび誘導体の注射や坐剤が用いられることが多い。タイやカンボジア国境付近ではアーテミシニンの効果が低下しているとの報告がある15)。マラロンの耐性株についても、アフリカで報告され始めるなど、マラリアの治療をめぐる状況は変化が激しい。現在、日本国内で販売されている抗マラリア薬は、スルファドキシン/ピリメタシン、メフロキン、塩酸キニーネ、アトバコン/プログラニル塩酸塩の4種類だが、このうち、予防投薬が認められているのは、メフロキンとアトバコン/プログラニル塩酸塩である。市販薬以外の抗マラリア薬については「熱帯病治療薬研究班(略称)」(http://www.ims.u-tokyo.ac.jp/didai/orphan)が保管している。熱帯熱マラリアを中心に、マラリアの治療や予防投薬については、国内の専門家会議からガイドラインが示されているが、実際の診療にあたっては、詳細は毎年更新される国際保健や旅行医学の文献で、最新の情報を入手して対処するのが望ましい16)17)。
感染症法における取り扱い(2012年7月更新)
全数報告対象(4類感染症)であり、診断した医師は直ちに最寄りの保健所に届け出なければならない。
届出基準はこちら
参考文献
- World Health Organization: World Malaria Report 2011. Genova, Switzerland. http://www.who.int/malaria/world_malaria_report_2011/en
- Tada Y et al. Travelers' risk of malaria by destination country: a study from Japan. Travel Med Infect Dis. 6 :368-72. 2008
- 大前比呂思,石川洋文. 気候変動と寄生虫症 -マラリアに焦点を当てて- 特集 気候変動と感染症 資源環境対策 44: 29-33. 2008
- 川合覚:人獣共通感染性・サルマラリアに関する最近の知見. モダンメディア 56:139-127. 2010
- 谷崎隆太郎 他 ヒトPlasmodium knowlesi 感染症(サルマラリア)の1例 IASR 34:6-7. 2013
- World Health Organization: Management of Severe Malaria, a practical guidebook, 2nd edition, 2000.Genova, Switzerland. http://www.rbm.who.int/docs/hbsm.pdf
- World Health Organization: Malaria Rapid Diagnostic Test Performance, 2011. Genova, Switzerland. http://www.finddiagnostics.org/.../Full-report-malaria-RDTs.pdf
- 大前比呂思 他 マラリア対策の進捗による感染状況の変化とフィールドでの迅速診断法の限界 臨床寄生虫学会誌18:76-79.2007
- Kimura M et al, Identification of the four species of human malaria parasites by nested PCR that targets variant sequences in the small subunit rRNA gene Parasitol. Inter. 46:91-95, 1997.
- Snounou, G et al. Identification of the four human malaria parasite species in field samples by the polymerase chain reaction and detection of a high prevalence of mixed infections. Mol. Biochem. Parasitol. 58:283-292, 1993.
- Sutherland, C et al. Two Nonrecombining Sympatric Forms of the Human Malaria Parasite Plasmodium ovale Occur Globally. J. Infect. Dis. 201:1544-1550, 2010.
- Singh B, et al. A large focus of naturally acquired Plasmodium knowlesi infections in human beings. Lancet 363:1017-1024, 2004.
- Imwong , et al. Spurious Amplification of a Plasmodium vivax Small-Subunit RNA Gene by Use of Primers Currently Used To Detect P. knowlesi. J. Clinical. Microbiol. 47:4173-7175, 2009.
- Baird JK et al. Diagnosis and treatment of Plasmodium vivax Malaria. Advances in Parasitology, vol 80, p204-270.
- Fairhurst, M. Artemisinin-Resistant Malaria: Research Challenges, Opportunities, and Public Health Implications. Am. J. Trop. Med. Hyg. 87:231-241. 2012.
- マラリア予防専門家会議 日本の旅行者のためのマラリア予防ガイドライン フリープレス 東京 2005
- World Health Organization: International Travel Health 2012 edition, Malaria Situation, 2012. Genova, Switzerland. http://www.who.int/ith